Le strutture degli acidi nucleici, come RNA e DNA, sono molto più di semplici sequenze; sono attori cruciali nell’attività biologica e nella regolazione genica. Comprendere come queste strutture interagiscono con proteine, altri acidi nucleici e composti sintetici è fondamentale non solo per svelare i meccanismi biologici, ma anche per guidare la scoperta e lo sviluppo di nuovi farmaci.
Nel mondo della ricerca biofarmaceutica, due approcci biofisici si stanno affermando come strumenti chiave per caratterizzare queste interazioni: la Calorimetria a Titolazione Isoterma (ITC) e la Grating-Coupled Interferometry (GCI). Vediamo come queste tecniche ci permettono di fare passi da gigante.
Calorimetria a Titolazione Isoterma (ITC): il “Gold Standard” per analisi in soluzione e label-free
La tecnica ITC è ampiamente riconosciuta come il “gold standard” per l’indagine delle interazioni molecolari. Il suo vantaggio principale è la capacità di fornire, in un unico esperimento, un profilo di legame completo che include:
- Affinità di legame (Kd)
- Variazioni di entalpia (ΔH)
- Variazioni di entropia (ΔS)
- Stechiometria (N)
Una caratteristica distintiva dell’ITC è che si tratta di una tecnica in soluzione, non è limitata dalle dimensioni delle macromolecole e, cosa fondamentale per gli studi strutturali, non richiede alcuna marcatura (labeling) dei campioni. Questo la rende ideale per valutare anche il corretto ripiegamento di un acido nucleico o di una proteina all’interno di un complesso.
Un esempio pratico dal nostro studio: Abbiamo utilizzato l’ITC per ottimizzare le condizioni di buffer, prevenendo interazioni non specifiche (NSB) del lividomicina con l’RNA genomico dell’HIV-1 e permettendo la cristallizzazione e la determinazione della struttura a raggi X del complesso RNA/farmaco, fondamentale per la progettazione di farmaci basata sulla struttura (Fig. 1).
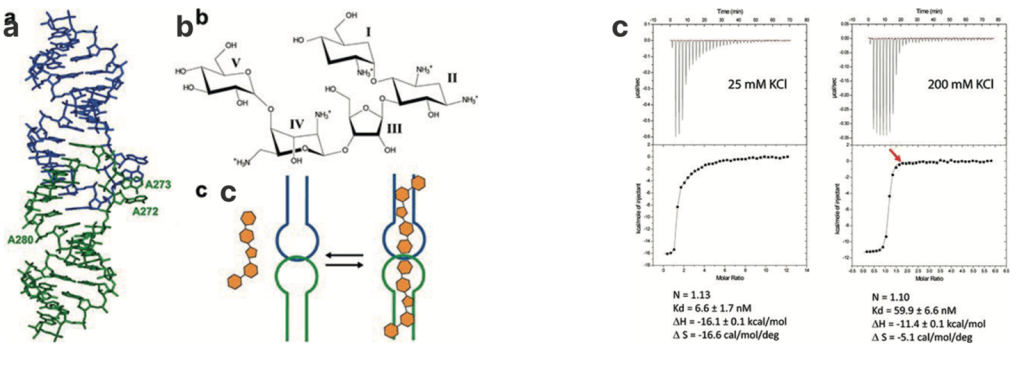
Figura 1
L’ITC si è rivelata cruciale anche per valutare il corretto ripiegamento dell’RNA di un riboswitch, essenziale per ottenere cristalli funzionali (Fig. 2).
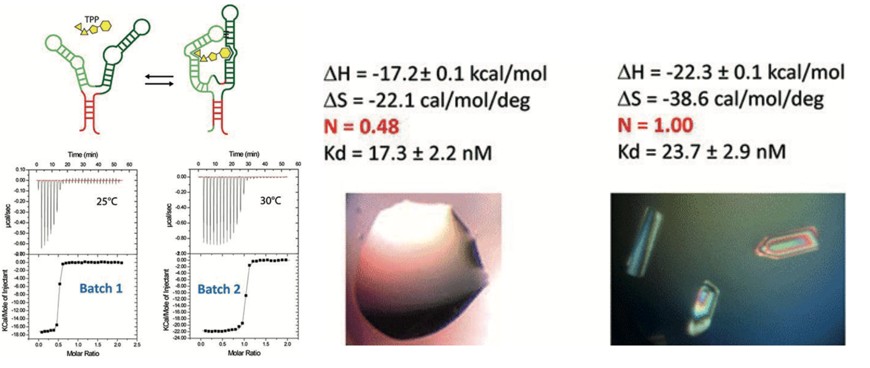
Figura 2
Grating-Coupled Interferometry (GCI): La Biosensoristica Label-Free per Cinetica e Affinità
La GCI è una tecnica di label-free basata su biosensori, eccellente per la caratterizzazione dell’affinità di legame (Kd) e della cinetica (kon e koff) delle interazioni tra una vasta gamma di materiali biologici e sintetici.
Come funziona? Quando le molecole target (come acidi nucleici o proteine) sono immobilizzate sulla superficie del sensore, il legame degli analiti porta a un aumento di massa e a un cambiamento nell’indice di rifrazione nel campo evanescente vicino alla superficie. La GCI misura questi cambiamenti dell’indice di rifrazione come segnali di variazione del pattern interferometrico dipendenti dal tempo. L’ampia superficie di interazione luce-campione della guida d’onda garantisce un rapporto segnale/rumore intrinsecamente elevato, per una sensibilità migliorata rispetto a tecniche analoghe come SPR e BLI. Inoltre, l’innovativa microfluidica no-clog consente l’uso di campioni grezzi e misurazioni di interazioni di legame in biofluidi e matrici complesse.
Applicazioni evidenziate nello studio:
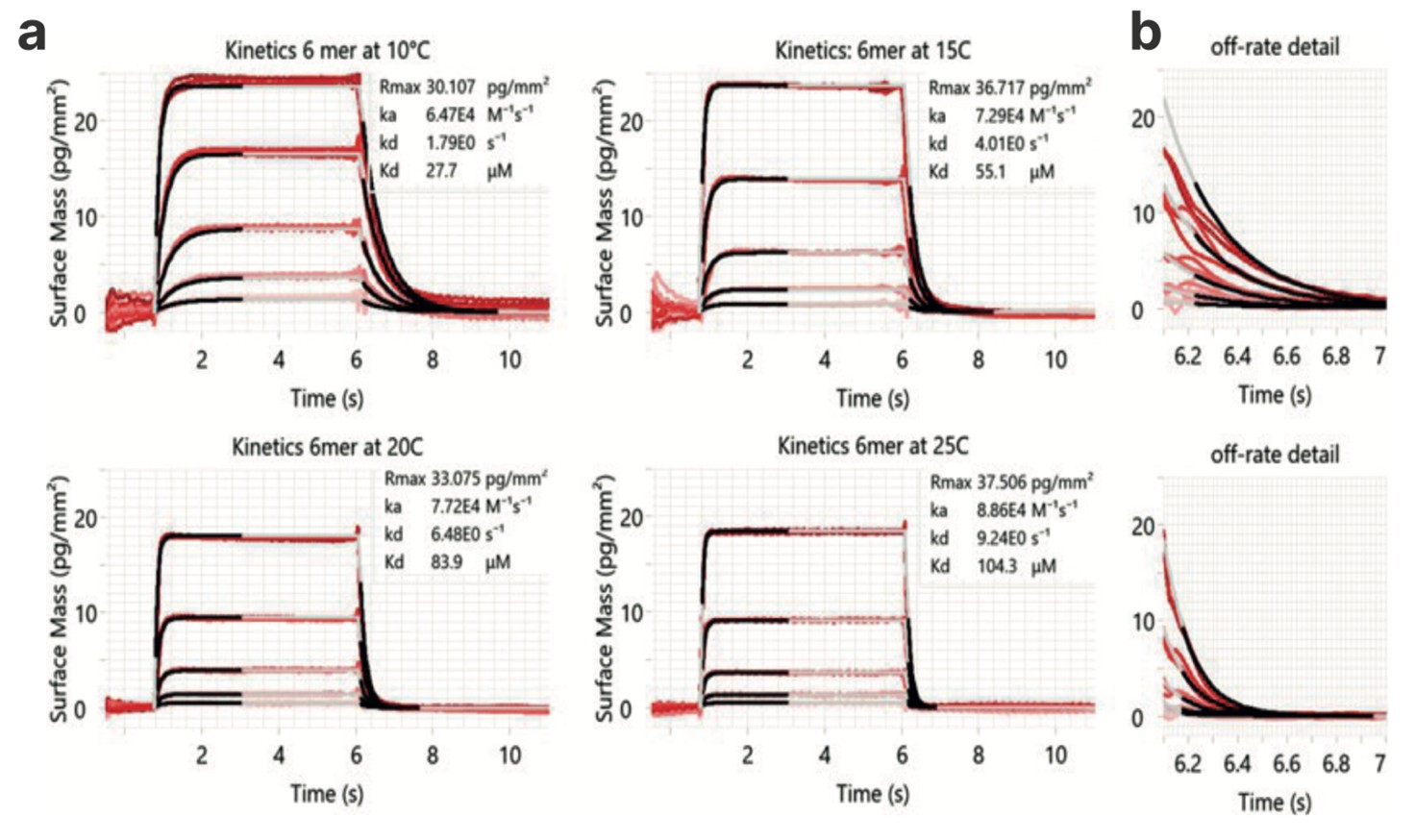
- Ibridazione DNA-oligo: Abbiamo utilizzato l’approccio multi-ciclo GCI per determinare con precisione l’affinità di legame e la cinetica dell’ibridazione di oligonucleotidi di DNA a singolo filamento, anche a diverse temperature e in matrici complesse (Fig. 3).
- Screening di frammenti: La tecnologia waveRAPID GCI si è dimostrata un mezzo veloce ed efficiente per identificare leganti a frammento per un riboswitch, coprendo un ampio intervallo di affinità.
- Riduzione dei tempi e del consumo di campione: Le analisi waveRAPID GCI hanno permesso di identificare rapidamente i leganti di frammenti per un riboswitch, riducendo significativamente i tempi e il consumo di campione

Figura 3
Conclusioni – Parola d’ordine complementarietà
Sia l’ITC che i biosensori GCI sono strumenti chiave per l’analisi delle interazioni in tutte quelle applicazioni che coinvolgono l’uso di acidi nucleici e oligonucleotidi. L’utilizzo sinergico dei dati ottenuti da ITC e GCI contribuisce ad aumentare il tasso di successo negli studi di biologia strutturale successivi su complessi RNA/DNA con proteine e ligandi naturali o sintetici.